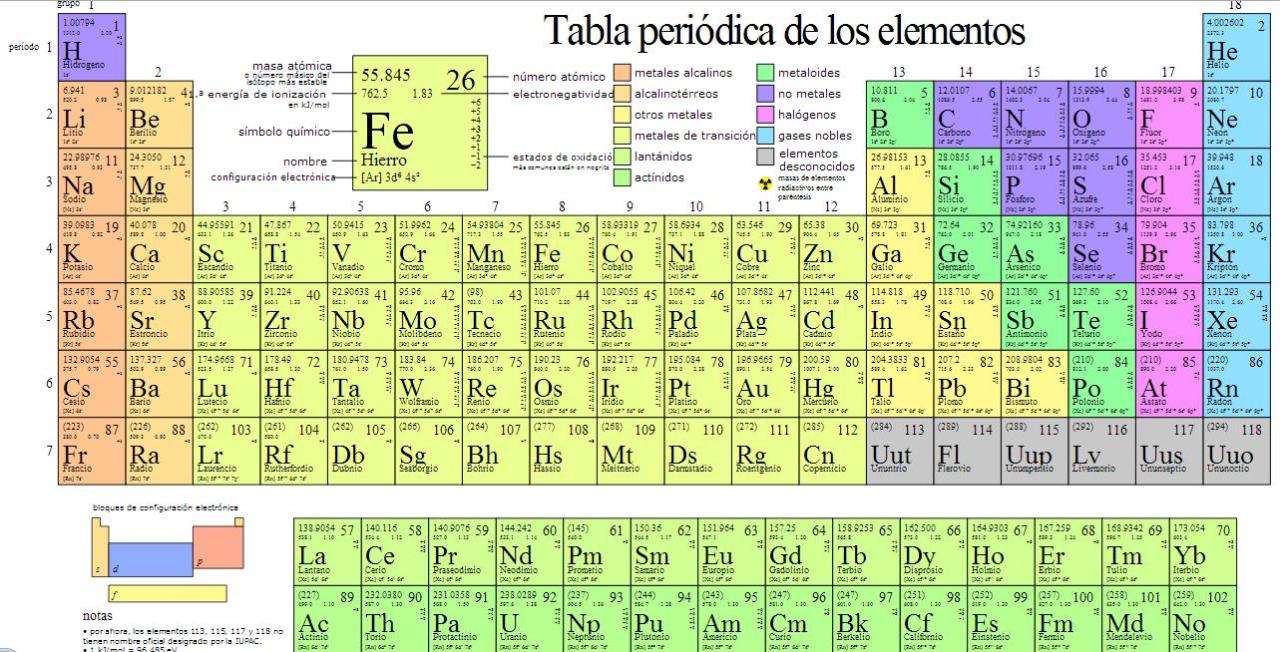
Si estáis aprendiendo la tabla periódica, os recomiendo el siguiente enlace "Tabla periódica", donde podéis hacerlo de una manera interactiva.
Hay cuatro etiquetas:
1. Tabla. Introducción
Donde acercando a cada elemento el cursor del ratón, os va dando información del mismo. Y si pincháis en él, se amplía más la información de cada uno de ellos.
2. Propiedades periódicas 1
Se centra en la explicación de los conjuntos de elementos químicos (metales, semimetales, no metales e inertes).
3. Propiedades periódicas 2
Aquí se centra en la explicación del tamaño de los átomos y la electronegatividad.
4. Construir la tabla
Éste es el apartado que más me ha gustado, pues sé que al principio resulta tedioso el aprenderse los elementos, su simbología, etc. Es un método más divertido que el clásico, así que os recomiendo que lo utilicéis.
También en cada una de las etiquetas hay actividades interactivas para que os ayuden a reforzar lo aprendido.